Очистка легкого углеводородного сырья от меркаптанов
В настоящее время вопрос сероочистки имеет наибольшую актуальность на Новокуйбышевском НХК, где перерабатывается широкая фракция легких углеводородов, содержащая значительные количества сернистых соединений. Пропановая и бутановая фракции ЦГФУ НХК после защелачивания удовлетворяют нормам МРТУ по содержанию сернистых, но эксплуатация проектной схемы очистки н-пентана 15-18%-ным раствором NaOH показала непригодность данного способа для удаления сернистых соединений.
Анализ сернистых соединений н-пентановой фракции ЦГФУ №2 методом потенциометрического титрования на рН-340 [1] и ГЖХ на приборе ЛХМ-8МД с селективным кулонометрическим детектором проточного типа [2] показал, что основную часть сернистых соединений в н-пентане составляют меркаптаны, из которых свыше 95% приходится на этилмеркаптан:
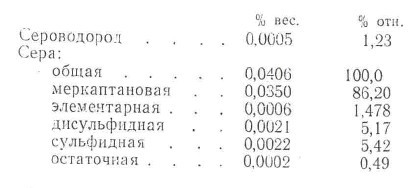
Таким образом, задача очистки н-пентана до норм МРТУ № 38-212-66 сводится к выделению меркаптанов. Опыты по извлечению меркаптанов и регенерации щелочных реагентов окислением кислородсодержащим газом проводились в аппарате с мешалкой [3] при 25°С. Экстракция тиоловых соединений из углеводородов щелочными растворами происходит по реакции [4]:
RSH + MeOH = RSMe + H2O + 12,6 ккал/моль.
Проведенные авторами опыты позволили установить, что степень превращения меркаптана в меркаптид не превышает 80-85% даже при применении 40%-ного водного раствора КОН и что скорость реакции при этом невелика. Равновесная степень превращения достигается за 15 мин при соотношении КОН:RH = 1:3, за 70 мин при соотношении КОН:RH = 1:6. Отсюда понятна причина неудовлетворительной работы узла очистки н-пентана раствором NaOH на ЦГФУ НХК, где время контакта фаз в эжекторном насосе очень мало, а концентрация щелочного раствора составляет не более 20%.
Повышение эффективности очистки от меркаптанов может быть достигнуто введением в систему полярных растворителей, которые, увеличивая растворимость меркаптанов в щелочах, оказывают большое влияние на положение равновесия за счет изменения активности реагирующих веществ [5]. В качестве таких растворителей были испытаны амины и амиды, производимые в промышленном масштабе (табл. 1).
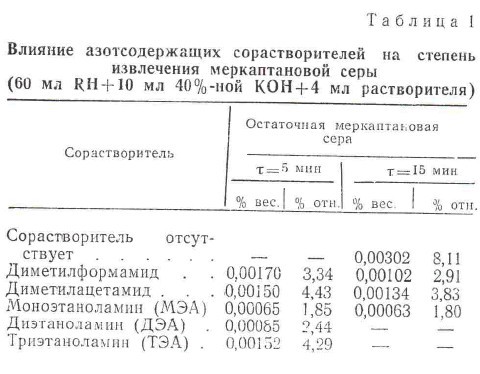
Введение азотсодержащих соединений в щелочной раствор повышает степень извлечения меркаптанов в 2-4 раза. Близкая к максимальной глубина очистки в присутствии МЭА достигается уже через 30 с (табл.2) вместо 30 мин при обработке 40%-ным раствором КОН.
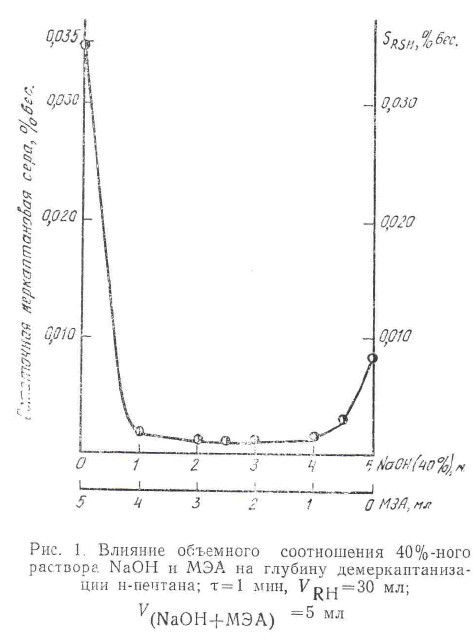
Наибольший эффект достигается при содержании МЭА в щелочном растворе от 40 до 60% (рис.1). Однако, учитывая относительно высокую стоимость МЭА по сравнению с NaOH, целесообразно принять 25%-ное содержание, т.е. соотношение NaOH:МЭА=4:1. При этом может с успехом применяться и 10-20%-ная щелочь.

Насыщенный меркаптанами МЭА-щелочной раствор можно регенерировать окислением меркаптидов в дисульфиды по реакции:
2RSNa + 0,5O2 + H2O (kt)? RSSR + 2NaOH,
идущей по анион-радикальному механизму [6,7].
Опыты по регенерации проводились при времени контекта 5 мин, концентрации катализатора 0,1% вес., концентрации RSNa 0,3% и скорости подачи воздуха 2 мин-1. Активными и стабильными катализаторами реакции окисления меркаптанов являются фталоцианины металлов переменной валентности [6,7]. В изученных условиях каталитическую активность проявляет только дисульфофталоцианин кобальта [C12H14O6N8S2CoNa2], 0,1%-ной концентрации которого достаточно для полного окисления этил-, пропил- и н-бутилмеркаптидов в течение 2 мин при комнатной температуре.
Разработанный авторами катализаторный комплекс может быть успешно применен для тонкой очистки широкой фракции легких углеводородов и бензинов от меркаптанов. Процесс эффективен как при низком (0,01 % вес. и менее), так и при высоком (3 % вес. и более) содержании меркаптанов в углеводородах и позволяет достичь практически полного удаления меркаптановой серы.
На основании результатов исследований для очистки индивидуальных углеводородов ЦГФУ НХК (в частности н-пентана) или всей широкой фракции легких углеводородов может быть предложена следующая принципиальная технологическая схема (рис.2)
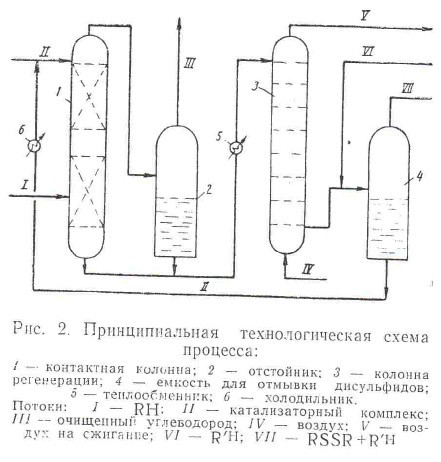 Очищаемый продукт н-пентан с температурой 15-35°С контактирует в контактной колонне 1 в противотоке с катализаторным комплексом (КТК) в соотношении 3:1 (лучше 1:1). В качестве контактной колонны может быть использована существующая колонна К-7 установки трикалийфосфатной очистки ЦГФУ. Время контакта – не менее 30 с. Катализаторный комплекс готовится растворением 1-3 кг катализатора в 1000 кг смеси NaOH (10-20%-ный раствор) и МЭА, взятых в соотношении 4:1. Меркаптаны превращаются в меркаптиды и переходят в щелочную фазу.
Очищаемый продукт н-пентан с температурой 15-35°С контактирует в контактной колонне 1 в противотоке с катализаторным комплексом (КТК) в соотношении 3:1 (лучше 1:1). В качестве контактной колонны может быть использована существующая колонна К-7 установки трикалийфосфатной очистки ЦГФУ. Время контакта – не менее 30 с. Катализаторный комплекс готовится растворением 1-3 кг катализатора в 1000 кг смеси NaOH (10-20%-ный раствор) и МЭА, взятых в соотношении 4:1. Меркаптаны превращаются в меркаптиды и переходят в щелочную фазу.
Очищенный от меркаптанов продукт в отстойнике 2 отделяется от щелочного раствора и отводится в парк товарной продукции, а насыщенный меркаптанами катализаторный комплекс нагревается в теплообменнике 5 до 40-60°С и поступает в верх колонны регенерации 3. В куб колонны подается воздух, находящийся в равном соотношении с КТК.
В колонне происходит окислительная регенерация КТК. Время контакта КТК с воздухом – не менее 5 мин. КТК после выхода из колонны 3 смешивается с частью неочищенной гексановой фракции ЦГФУ в соотношении 4:1 и поступает в отстойник емкость для отмывки от дисульфидов 4. Дисульфиды нерастворимы в КТК, они полностью переходят в углеводородный слой и удаляются вместе с гексановой фракцией. Кроме того, при смешении гексановой фракции с КТК происходит окисление растворенным в щелочном растворе кислородом меркаптанов, содержащихся в гексановой фракции. Тем самым достигается одновременная очистка щелочного раствора от кислорода и гексановой фракции от меркаптанов. При необходимости дисульфиды могут быть выделены из КТК простым отстаиванием, без применения углеводорода для отмывки. Регенерированный КТК из отстойника-емкости 4 через холодильник 6, где он охлаждается до 15-20°С, возвращается в систему.
ЛИТЕРАТУРА
1. Щербина Е.И. и др., ЖПХ, 1971, 44, №7.
2. Кричмар С.И., Степаненко В.Е., ЖАХ, 1969, №12.
3. Мазгаров А.М. Автореф.дис. на соиск. учен. степ. канд. хим. наук, МХТИ им. Менделеева, 1970.
4. Соколина Л.Д. и др. В сб.: «Газовая промышленность», 1971, №11.
5. Герасимов Я.И. и др. Курс физической химии, т.1, М., «Химия», 1969, с.271.
6. Кундо И.Н., Кейер Н.П., ЖФХ, 1968, 42, №6.
7. Thomas I. Wallace et al. Ind. Engng. Chem., 1964, 56, N 7, p. 121.